李氏大药厂(0950.HK):研发进入收获期,发展迈入快车道
作者:格隆汇 夏以勋
2019年3月28日下午,李氏大药厂(950.HK)在香港举办业绩会,公布其2018财年业绩。公司执行董事兼行政总裁李小羿博士、CFO邹耀明先生出席会议。

2018财年,公司录得营收11.38亿港元,同比增长12.8%,六种主要产品贡献94.0%的收益,基本与2017年持平;毛利率65.6%,公司拥有人应占纯利4.18亿港元,同比增长79.9%,纯利率36.8%。董事会建议派发末期股息每股0.084港元。
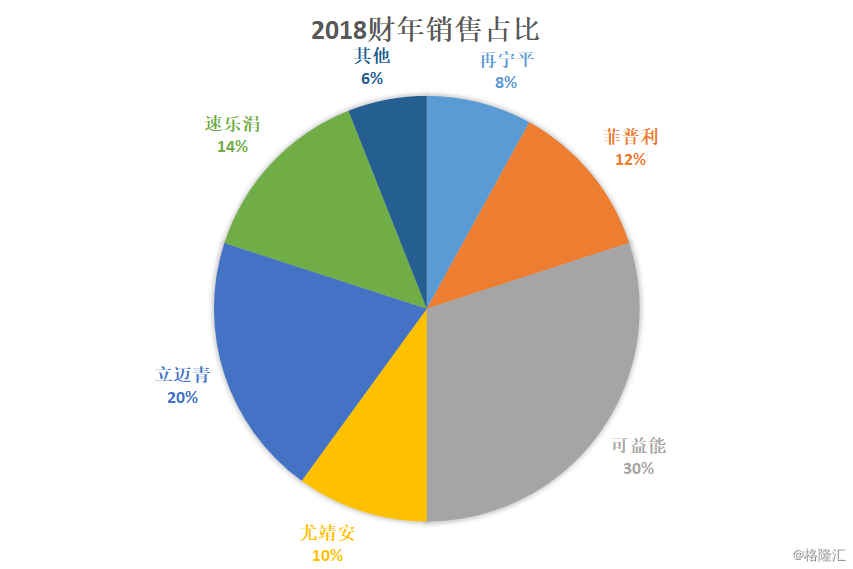
引进产品的销售额达到6.18亿港元(占总收入的54.3%),同比增长13.5%,其中再宁平录得8627.4万元(占总收入的8%),同比增长46.6%;菲普利录得1.42亿元(占总收入的12%),同比增长24.1%;可益能录得3.37亿元(占总收入的30%),在年内保持平稳。
专利产品的销售额达到5.19亿港元(占总收入的45.7%),同比增长增长11.9%,尤靖安首次突破1亿港元录得1.15亿元(占总收入的10%),同比增长22.8%;立迈青录得2.25亿元(占总收入的20%),同比增长7.4%;速乐涓录得1.63亿元(占总收入的14%),同比增长9.6%;睿保特同比增长36.8%。
研发开支2.9亿港元,占年度收益的25.5%,其中1.53亿港元已确认为费用,而1.37亿港元已资本化为无形资产。
新药方面,2018年7月,Sancuso(格拉司琼透皮系统)取得中国药监局的批准;公司获得Sancuso在中国(不包括北京、上海及广州)作商业化和推广的独家许可权。Sancuso是世界上第一种亦是唯一一种5-HT3受体拮抗剂的透皮贴剂,用于预防接受中度或高度致吐化疗方案的患者的噁心和呕吐。期内,公司已经呈交三项药物进口许可证申请,曲唑酮、Prulifloxacin及INOMax。其中,Prulifloxacin已成功获中国药监局完成临床审核,而INOMax则获得豁免进行临床研究。另外,公司呈交四项新药申请,分别是苯丁酸钠药片、苯丁酸钠粉剂、曲前列环素及磺达肝癸钠。其中,苯丁酸钠粉剂已获取完整回应函件,公司将于2019年6月底之前提交补充数据供最终审批。
生产基地方面,合肥生产基地的脂质体生产线及生物制剂药物生产线的建设已经完成,新实验室动物中心已开始运作,可对表面活性剂、小牛血液提取物或蛇毒提取物等产品进行各种动物试验。南沙生产基地已经于2018年7月取得多剂量生产线的生产许可,于2018年9月取得采用吹灌封技术的单剂量生产线的生产许可,并与2018年10月取得了细胞毒口服胶囊的生产许可。
以下为提问环节
Q1、2019年新品种上市的时间?为上市有做什么准备?
A1、目前在ANDA,NDA或者IDL在准备递申请的大概有20个,已经在审评中的有10个,这些都是很快会出来的。Sancuso今年三月已经正式开始销售,Probiotics VSL#3和Dicoflor下个月也会上市,瑞莫杜林仿制药也会上市等,会有很多品种上市。Probiotics VSL#3要highlight一下,这益生菌有4500亿个细菌,现在国内最好的品牌大概有60亿个细菌,这是重大的差别,有很多文献支持的益生菌,在美国已卖的很好,益生菌是上百亿的市场,在中国的增长很快,益生菌没有两票制等影响,在公司已经建立的代理渠道上运用,大家都很期待这个产品,是公司未来重点发展的产品。瑞莫杜林高血压团队已经销售,INOMax已经获得豁免进行临床研究,销售团队用瑞莫杜林的团队来做,很有经验了,因为很多肺动脉高压都是出现在静脉手术,术前术中术后,INOMax市场调研反响很好,因为国内现在主要用工业一氧化氮,会有比较多的问题,目前产品经理等都到位了,在做准备工作。
瑞莫杜林已经能做到近4000万,最大的问题是价格,很多人用不起,在美国是6个亿美金销售的产品,在中国病人只能有两个星期,在美国一年都用,所以现在李氏大药厂做仿制,可以把价格做下来进入医保,国家现在对罕见病非常的重视,进入医保是完全可能。这个药的仿制在美国刚刚批准,Sandoz的API supplier跟李氏大药厂的API supplier是一家的,这个药很难合成,没有很多药企能做出来,这也是公司只做高端仿制,上市可以用现有的团队做起来。
阿齐沙坦,再加上肾素抑制剂(阿利吉仑)和再宁平(乐卡地平),基本覆盖了高血压的主要作用机制。阿齐沙坦恒瑞是第一家,一致性评价很难做,恒瑞的BE登记了2次,还没通过,李氏大药厂现在是第二家报。
到年底,公司应该会有10个产品,都有很大的市场价值。
Q2、资本市场有没有新的情况,科创板或者是香港未盈利生物科技板块?
A2、中国肿瘤医疗有限公司(COF,China Oncology Focus)有机会上科创板,现在在做A轮的融资。眼科公司,A轮的融资希望会在下个月完成,很多投资人都在关注,到目前为止比较全面的眼科公司,既有生产又有研发,希望在年底会有一轮pre-IPO,明年计划在香港上市。还有一家器械公司,也会有所考量。选择上市,Biotech公司的价值会呈现出来,最终也会反映到上市公司中。
Q3、近期要上的品种,市场空间的预判?峰值大概多少?
A3、近期要上的药,其实都比目前公司在卖的药更有市场空间,瑞莫杜林做仿制的话,如病人从2个月到12个月已经有6倍的增量,价格如果减一半,也可以涨3倍,市场推广空间很大,很多病人用了效果不错,但是没有钱再用了,之后病情又进行反复就出现很多问题。
新药中,比如INOMax是个10亿市场空间的品种,另外公司也有卖器械等,这些领域就不太会受现在的政策影响。
过去5年,公司不断扩展自己的能力,能做高端仿制药,能做技术转移,现在fundamental difference是看到一个机会,能去做,也能去做成功,比如Surfactant正在申请,把美国的生产转移到合肥,这很难,Surfactant是自Windtree引进,FDA批准的首个治疗NRDS全合成药物,是个脂质体。
公司也很快会出那曲肝素,公司也报了一个合成的肝素,以前的合成肝素的市场很小,几乎是3倍低分子肝素,现在低分子肝素由于变了名,比如那曲肝素、达肝素,全部价格都变高了,所以现在是不到一半的价格, 公司的合成肝素很有竞争力。合成肝素合成技术比较难,现在报的就是恒瑞,公司也会去做,这个药物上来就是医保药物,开发会很快。
未来,益生菌也是公司的重点,VSL#3是益生菌中的原子弹,如果菌数不够,经过胃等细菌不够,VSL#3有4500亿菌,是很厉害的。
Q4、亮丙瑞林是同样对标丽珠的微球技术吗?技术是从哪些地方来的?丽珠当年是从武田继承过来的,微球的技术壁垒还是比较高的,公司目前微球还处于研发后期,那么如何处理后续的大规模生产问题?
A4、公司的亮丙瑞林是来自于一家西班牙的公司,已经是FDA批准了,做到最后1个月,武田的已经向上,而公司的这款还可以持续,公司因此还延长了follow-up,看到它的抑制还是很彻底。公司未来也会报3个月的。
Q5、未来license-in 和 license-out的考虑?
A5、最近拿下的license-in是治疗妇女绝经后的阴d干涩症,现在一般做的都是含雌性激素,在美国就有可能会引起内膜癌,乳癌等,需要有Black Box Warning,所以在国内药用的很少,公司引进的是美国刚刚在2017年批准的药,在欧洲是2018年才批准,不含雌性激素,随着老龄化增强,市场需求还是比较大。license-in主要以高端仿制和技术转移为主,过去几年投入的品种,近期也会上市,从去年公司就开始培养销售团队,让他们可以承接这些产品,从大药厂也引进了不少的人才。
财经号声明: 本文由入驻中金在线财经号平台的作者撰写,观点仅代表作者本人,不代表中金在线立场。仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。同时提醒网友提高风险意识,请勿私下汇款给自媒体作者,避免造成金钱损失,风险自负。如有文章和图片作品版权及其他问题,请联系本站。



