Gut | 发现MOTS-c有助于其在HBV感染期间的抗病毒
乙型肝炎病毒(HBV)感染对线粒体活性造成实质性损害,这阻碍了慢性乙型肝炎(CHB)有效治疗方法的发展。线粒体来源的短肽MOTS-c具有多种生物活性,为治疗HBV感染提供了一种有希望的新方法。
2023年10月3日,福建医科大学欧启水、刘灿及山东大学冉宁共同通讯在Gut(IF=25)在线发表题为“Novel function of MOTS-c in mitochondrial remodelling contributes to its antiviral role during HBV infection”的研究论文,该研究表明MOTS-c在线粒体重塑中的新功能有助于其在HBV感染期间的抗病毒作用。
MOTS-c与HBV DNA表达呈负相关(R=-0.71),其区分CHB与健康对照的AUC(曲线下面积)为0.9530,IA(免疫反应性)与IC(非活性HBV携带者)的AUC为0.8689。在体外或体内观察到抑制HBV复制(抑制率为50 - 70%)和改善肝功能的同时,没有明显的毒性。研究发现,MOTS-c可促进线粒体生物发生并增强MAVS(线粒体抗病毒信号蛋白)信号通路。这种影响取决于MOTS-c调节MYH9 -actin介导的线粒体稳态的能力。MOTS-c有潜力作为HBV感染进展的生物标志物,同时也能增强抗病毒疗效。这些发现为有效治疗慢性乙型肝炎患者提供了一种有希望的创新方法。此外,该研究揭示了MOTS-c在调节MYH9-actin介导的线粒体动力学和促进线粒体生物发生中的新作用。

乙型肝炎是一种病毒感染,攻击肝脏,导致持续和慢性疾病,如肝功能衰竭和肝细胞癌。全世界每年有150万新的乙型肝炎感染病例。慢性乙型肝炎(CHB)期患者采用抗病毒药物治疗,而其他阶段的慢性乙型肝炎病毒(HBV)感染患者采用不同的治疗方法。然而,肝活检的要求对CHB具体分期的诊断提出了挑战目前治疗慢性HBV感染的方法复杂且缺乏疗效,导致大多数患者需要长期治疗。因此,发现新的方法来改善HBV感染的诊断和治疗CHB患者对于确定有效的治疗方法至关重要。线粒体通过启动抗病毒先天免疫监视和免疫反应在HBV感染的进展中起重要作用。线粒体抗病毒信号蛋白(MAVS)定位于线粒体膜,是调控线粒体介导的HBV感染免疫应答的关键因素,是线粒体与丝裂原活化蛋白激酶(MAPK)信号通路和核因子κ b (NF-κB)信号通路之间的桥梁。病毒可以劫持线粒体过程,通过提高活性氧(ROS)水平、减少能量供应和破坏线粒体结构,导致它们功能失调,从而削弱细胞及其抵抗HBV感染的能力。线粒体损伤是HBV感染的一个标志,也是HBV难以治疗的主要原因之一。
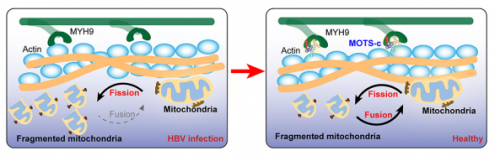
MOTS-c在MYH9-actin分子复合物介导的线粒体动力学中的作用示意图(图源自Gut )肌凝蛋白和肌动蛋白形成典型的分子运动复合物,通过调节线粒体裂变/融合动力学来维持线粒体稳态和细胞存活。线粒体裂变/融合过程的失调与细胞应激密切相关,并与各种人类疾病有关。然而,HBV感染期间线粒体动力学调节的机制仍不清楚。MOTS-c是一种16个氨基酸的生物活性肽,来源于线粒体12S rRNA的开放阅读框,可在多种组织中检测到,包括肝脏、肌肉和循环。因此,它被称为“线粒体激素”或“线粒体因子”。MOTS-c已经在临床试验中进行了测试,由于其潜在的治疗作用,已被证明在治疗各种疾病方面是安全有效的,包括肥胖、心血管疾病和癌症。该研究发现血清MOTS-c与HBV DNA水平呈显著负相关,对不同HBV感染阶段具有良好的诊断价值。外源性MOTS-c可增强HBV感染小鼠肝脏和HBV感染细胞中的HBV复制抑制。重要的是,重复使用MOTS-c剂量(500µg)治疗HBV感染的C3H/He小鼠显示出HBV抑制作用,在没有可检测到的毒性的情况下显著改善功能。MOTS-c的治疗效果可归因于MOTS-c引发的MAVS信号通路激活增加,这反过来又通过MOTS-c依赖的线粒体动力学介导的线粒体生物发生升高,而线粒体生物发生是由MYH9 -肌动蛋白分子复合物调节的。这些发现为MOTS-c在调节线粒体动力学中的作用以及HBV感染和其他线粒体相关疾病的重要诊断和治疗意义提供了重要见解。原文链接:https://gut.bmj.com/content/early/2023/10/03/gutjnl-2023-330389
财经号声明: 本文由入驻中金在线财经号平台的作者撰写,观点仅代表作者本人,不代表中金在线立场。仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。同时提醒网友提高风险意识,请勿私下汇款给自媒体作者,避免造成金钱损失,风险自负。如有文章和图片作品版权及其他问题,请联系本站。


